Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
北畠 里実*; 後田 藤太*; 平山 亮一*; 古澤 佳也*; 舟山 知夫; 横田 裕一郎; 岡畑 恵雄*; 伊藤 敦*
JAEA-Review 2014-050, JAEA Takasaki Annual Report 2013, P. 86, 2015/03
高LETイオンビームの特異な生物作用は、その飛跡に沿ったエネルギー付与分布のトラック構造が原因であると言われている。そこで、トラック構造を構成するコア領域とペナンブラ領域それぞれの生物作用を明らかにするために、それらがDNAに誘発する損傷の可視化を行った。本研究では、不溶性DNAシートの作製プロトコルを確立すると共に、高LETイオンビームで照射した後に生じる代表的なDNA酸化損傷である8-ヒドロキシグアニンの分布の可視化を試みた。実験では、不溶性DNAシートを原子力機構TIARAのプロトンおよびネオンイオンビームで照射した後、8-ヒドロキシグアニン特異的抗体と蛍光二次抗体で処理することで損傷の可視化を試みた。予備的な実験の結果では、照射したDNAシート上にドット状の蛍光が観察され、これがイオン照射で生じたDNA損傷由来である可能性が示唆された。
高橋 昭久*; 久保 誠*; Ma, H.*; 中川 彰子*; 吉田 由香里*; 磯野 真由*; 金井 達明*; 大野 達也*; 古澤 佳也*; 舟山 知夫; et al.
Radiation Research, 182(3), p.338 - 344, 2014/09
被引用回数:57 パーセンタイル:90.56(Biology)DNA二本鎖切断(DSB)は相同組換え(HR)と非相同末端結合(NHEJ)により修復される。重粒子線治療における放射線増感剤の標的候補を明らかにすることを目的とした。がん抑制遺伝子p53欠損マウス胚線維芽細胞由来の野生型細胞, HR修復欠損細胞, NHEJ修復欠損細胞,二重修復欠損細胞を用いた。各細胞にX線,炭素線,鉄線,ネオン線,アルゴン線を照射し、コロニー形成法で生存率を調べた。10%生存率線量値(D10値)を用いて、増感比は(野生型細胞のD10値)/(修復欠損細胞のD10値)の式で算出した。D10値はいずれの線質においても、野生型細胞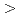 HR修復欠損細胞
HR修復欠損細胞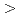 NHEJ修復欠損細胞
NHEJ修復欠損細胞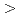 二重修復欠損細胞の順に低くなった。HR修復欠損による増感比はLET無関係に一定で約2であった。一方、NHEJ修復欠損の増感比はLETが高くなるに従い減少するものの、HR修復欠損よりも高い増感効果を示した。高LET放射線の高RBEの要因はNHEJ修復の抑制と誤修復であり、炭素線における増感剤の主要な標的候補はNHEJ修復であることが示唆された。
二重修復欠損細胞の順に低くなった。HR修復欠損による増感比はLET無関係に一定で約2であった。一方、NHEJ修復欠損の増感比はLETが高くなるに従い減少するものの、HR修復欠損よりも高い増感効果を示した。高LET放射線の高RBEの要因はNHEJ修復の抑制と誤修復であり、炭素線における増感剤の主要な標的候補はNHEJ修復であることが示唆された。
舟山 知夫; 和田 成一; 小林 泰彦; 渡辺 宏*
Radiation Research, 163(2), p.241 - 246, 2005/02
被引用回数:32 パーセンタイル:64.71(Biology)重イオンの生物作用を解明を目的に、細胞を一つ一つ重イオンで照射することができるマイクロビームシステムを確立した。イオン飛跡検出用プラスチックCR-39で作った照射容器で培養したCHO-K1細胞を蛍光染色で自動認識し、その位置座標をもとに、細胞を個別に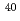 Ar
Ar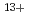 イオンで照準照射した。照射後、照射容器の底のCR-39の裏側を37
イオンで照準照射した。照射後、照射容器の底のCR-39の裏側を37 Cのアルカリエタノール溶液で処理し、細胞を生かしたまま飛跡を可視化することに成功した。可視化した飛跡と、細胞の顕微鏡画像を重ね合わせ、細胞にヒットしたイオンの数の位置を正確に検出した。アルゴンイオンで照射した細胞では、照射による細胞増殖の阻害が引き起こされていた。加えて、細胞核にアルゴンイオンが一つヒットしただけで、細胞の増殖が非常に強く阻害されることを明らかにした。
Cのアルカリエタノール溶液で処理し、細胞を生かしたまま飛跡を可視化することに成功した。可視化した飛跡と、細胞の顕微鏡画像を重ね合わせ、細胞にヒットしたイオンの数の位置を正確に検出した。アルゴンイオンで照射した細胞では、照射による細胞増殖の阻害が引き起こされていた。加えて、細胞核にアルゴンイオンが一つヒットしただけで、細胞の増殖が非常に強く阻害されることを明らかにした。
小林 泰彦; 舟山 知夫; 和田 成一; 古澤 佳也*; 青木 瑞穂*; Shao, C.*; 横田 裕一郎; 坂下 哲哉; 松本 孔貴*; 柿崎 竹彦; et al.
宇宙生物科学, 18(4), p.235 - 240, 2004/12
銀河宇宙線のように、低フルエンス・低フルエンス率の高LET重イオン(粒子線)による生物影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、高エネルギー重イオンマイクロビームを顕微鏡観察下の生物試料に照射するために原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射・観察する実験系を開発した。標的細胞を貫通したイオンのエネルギーと個数をシンチレータ/フォトマルを用いて測定することによって、重イオンを1個ずつカウントしながら正確に照射することが可能となった。さらに、CR-39を直ちに37 Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。国内外の重粒子線のマイクロビーム開発の歴史を概観し、細胞核へのシングルイオンヒット効果やバイスタンダー効果に関する最近の研究成果をレビューする。
Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。国内外の重粒子線のマイクロビーム開発の歴史を概観し、細胞核へのシングルイオンヒット効果やバイスタンダー効果に関する最近の研究成果をレビューする。
小林 泰彦; 舟山 知夫; 和田 成一; 坂下 哲哉
宇宙生物科学, 18(3), p.186 - 187, 2004/11
銀河宇宙線のように、低フルエンス率の高LET重イオン(粒子線)による生物影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射し、その影響を経時的に観察する実験システムを開発している。今回、照射前に試料を自動スキャンして細胞を検出するオフライン顕微鏡及び取得した座標データに従ってビーム位置に標的細胞を移動するオンライン顕微鏡の各々の試料ステージ更新し、従来は 10
10 m以上の誤差があった試料移動の位置再現精度が
m以上の誤差があった試料移動の位置再現精度が 1
1 mに向上したことにより、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験結果について報告する。
mに向上したことにより、多数の標的細胞を次々に自動照準して連続的にシングルイオン照射することが可能になった。併せて、最近の細胞照射実験結果について報告する。
小林 泰彦; 舟山 知夫; 和田 成一*; 田口 光正; 渡辺 宏
Radiation Research, 161(1), p.90 - 91, 2004/01
低線量放射線の生物影響、特に低フルエンス・低フルエンス率の高LET重イオン(粒子線)による影響を明らかにするためには、マイクロビームを用いた細胞照射実験が有効な手段となる。そこで、高エネルギー重イオンマイクロビームを顕微鏡観察下の生物試料に照射するために原研・高崎研・バイオ技術研究室で開発した細胞局部照射装置を用いて、哺乳動物培養細胞を個別に重イオンで照射・観察する実験系を開発した。標的細胞を貫通したイオンのエネルギーと個数をシンチレータ/フォトマルを用いて測定することによって、重イオンを1個ずつカウントしながら正確に照射することが可能となった。さらに、CR-39を直ちに37 Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。
Cでエッチングして各標的細胞における実際のイオン飛跡を可視化すると同時に、その飛跡が可視化されたCR-39上で細胞の照射後培養と観察を継続する方法を確立した。
舟山 知夫; 和田 成一; 小林 泰彦
Radiation Research, 161(1), p.111 - 112, 2004/01
原研高崎TIARAに設置された生物照射用マイクロビーム装置を利用して哺乳動物細胞を個別に照射・観察する方法を確立した。照射する細胞にはCHO-K1細胞をもちいた。細胞を照射2時間前にイオン飛跡検出器CR-39(100 m厚)で作製した照射容器にまきこみ、接着を確認したのち照射にもちいた。照射直前に、試料より培地を除き、乾燥を防止するため薄いカプトンフォイル(8
m厚)で作製した照射容器にまきこみ、接着を確認したのち照射にもちいた。照射直前に、試料より培地を除き、乾燥を防止するため薄いカプトンフォイル(8 m厚)で試料をカバーし、その後、11.5MeV/u 40Ar (LET=1260 keV/
m厚)で試料をカバーし、その後、11.5MeV/u 40Ar (LET=1260 keV/ m)で細胞核を狙ったマイクロビーム照射をおこなった。照射後、細胞にヒットしたイオン数及び位置,細胞生存に影響を与えない新開発の手法で検出し、その後、照射後60時間まで継続的にそれぞれの細胞の増殖を観察した。個々の細胞に対して検出した照射イオン数・位置と、各細胞の増殖曲線を比較したところ、Arイオンがシングルヒットした細胞ではヒットしていない細胞に比べ極めて強い細胞増殖の阻害がおこっていることが確かめられた。
m)で細胞核を狙ったマイクロビーム照射をおこなった。照射後、細胞にヒットしたイオン数及び位置,細胞生存に影響を与えない新開発の手法で検出し、その後、照射後60時間まで継続的にそれぞれの細胞の増殖を観察した。個々の細胞に対して検出した照射イオン数・位置と、各細胞の増殖曲線を比較したところ、Arイオンがシングルヒットした細胞ではヒットしていない細胞に比べ極めて強い細胞増殖の阻害がおこっていることが確かめられた。
小林 泰彦; 舟山 知夫; 和田 成一; 田口 光正; 渡辺 宏
Nuclear Instruments and Methods in Physics Research B, 210(1-4), p.308 - 311, 2003/09
重イオンマイクロビームは、放射線の生物作用研究のための新しいツールとして極めて有望である。原研・高崎研では、銀河宇宙線のような極低フルエンス高LET重粒子線の生物影響の解明、特にトラック構造の局所的エネルギー付与分布による影響をダイレクトに解析することを目指して、サイクロトロンから得られる比較的高エネルギーの重イオンマイクロビームを用いて哺乳動物培養細胞を個別に照射・観察する実験系を開発した。その結果、ArやNeなどの重イオン1個のヒットで細胞の増殖が強く抑制されることを見いだした。
小林 泰彦; 舟山 知夫
Isotope News, (590), p.2 - 7, 2003/06
マイクロビームによる局部照射は放射線の生物作用研究のための新しいツールとして極めて有望と考えられる。1個のイオン、特にネオンやアルゴンのような重イオンを1個、細胞に狙い撃ちして照射すると細胞がどうなるか。プロトンあるいはヘリウムイオンのような軽イオンの場合と異なり、重イオン1個のヒットで細胞は完全に不活化することが最近明らかになった。原研などで現在進行中であり、世界の各地でも計画が目白押しのマイクロビーム細胞照射実験について、その歴史と現状を概説するとともに、イオン1個のヒットが細胞に引き起こす現象について最近の成果を紹介する。
和田 成一; 夏堀 雅宏*; 伊藤 伸彦*; 舟山 知夫; 小林 泰彦
Nuclear Instruments and Methods in Physics Research B, 206, p.553 - 556, 2003/05
被引用回数:3 パーセンタイル:27.66(Instruments & Instrumentation)宇宙環境における高LET重粒子線被曝の生物影響を解明するためには、低線量・低フルエンスの重イオン照射によって細胞に誘導されるDNA損傷を正しく解析する必要がある。しかし、低フルエンスの重イオンはランダムにヒットするため、細胞に対する重粒子1個の生物学的効果を直接に検出することはこれまで困難だった。そこで、個々の細胞ごとのDNA損傷を評価することが可能なコメットアッセイ法を用いるとともに、同時に各細胞での重イオンのヒット位置を飛跡検出器CR-39を用いて直接に検出することが可能な方法を開発し、動物培養細胞の核にヒットしたイオン粒子数と、その細胞に生じたDNA損傷の程度を同時に検出する方法を確立した。そして、異なるLET値を有するいくつかの重粒子線照射によって細胞に誘導されたDNA損傷を定量的に解析し、照射したイオンのLET値との関連を解析した。
 -radiation
-radiation横谷 明徳; Cunniffe, S. M. T.*; Stevens, D. L.*; O'Neill, P.*
Journal of Physical Chemistry B, 107(3), p.832 - 837, 2003/01
被引用回数:26 パーセンタイル:56.36(Chemistry, Physical)相対湿度を制御した条件下で、プラスミドDNAに対して 線を照射した後、FpgとNthという二つの塩基除去修復酵素をプローブとして用いて、DNAの鎖切断,塩基損傷及びこれらを含むクラスター損傷の収率を測定した。相対湿度を0
線を照射した後、FpgとNthという二つの塩基除去修復酵素をプローブとして用いて、DNAの鎖切断,塩基損傷及びこれらを含むクラスター損傷の収率を測定した。相対湿度を0 98%まで変えることで、DNAに配位している水和水の量を、5
98%まで変えることで、DNAに配位している水和水の量を、5 38分子/ヌクレオチドまで変えることができるため、
38分子/ヌクレオチドまで変えることができるため、 線のDNA損傷に与える水和水の効果を調べることができる。得られた結果は、鎖切断に関しては
線のDNA損傷に与える水和水の効果を調べることができる。得られた結果は、鎖切断に関しては 線照射の場合のそれとほとんど同じであったのに対して、酵素処理により検出される塩基損傷はほとんど観測されなかった。以上の結果から、高LET放射線である
線照射の場合のそれとほとんど同じであったのに対して、酵素処理により検出される塩基損傷はほとんど観測されなかった。以上の結果から、高LET放射線である 線により、DNA修復酵素が修復できないような複雑なクラスター損傷が生成している可能性が示された。
線により、DNA修復酵素が修復できないような複雑なクラスター損傷が生成している可能性が示された。
舟山 知夫; 小林 泰彦
放射線生物研究, 37(3), p.334 - 347, 2002/09
マイクロビーム装置は、微小なサイズの放射線プローブを利用して、照射対象の一部分に放射線を照射し、それによるエネルギー付与を利用して、対象試料の解析や微細加工をおこなうためのツールである。生物試料に対するマイクロビーム技術の応用は、マイクロPIXEや、ラジオマイクロサージャリー、そして、放射線生物効果の解析等に利用されてきている。原研高崎では、重イオンマイクロビーム装置製作と、それをもちいた生物応用技術の開発をこれまでおこなってきた。しかし、この装置をもちいたこれまでの生物試料照射は、主にラジオサージャリー技術が中心であり、放射線生物研究ツールとしては利用されてこなかった。これは、高LET・高エネルギーのイオンビームを利用することに伴う、いくつかのビーム技術的制約及び単一細胞の自動認識・標的システムの開発上の制約によるものであった。原研高崎の重イオンマイクロビーム装置でも、培養細胞照射実験系が確立し、放射線生物研究ツールとして活用ができるようになった。この原研高崎の生物照射用マイクロビーム装置の概要と、培養細胞照射の実際の過程について概説する。
小林 泰彦
放射線生物研究, 37(1), p.67 - 84, 2002/03
マイクロビームによる局部照射は、放射線の生物作用研究のための新しいツールとして極めて有望である。原研・高崎研では、銀河宇宙線のような極低フルエンス高LET重粒子線の生物影響の解明、特にトラック構造の局所的エネルギー付与分布による影響をダイレクトに解析することを目指して、サイクロトロンから得られる比較的高エネルギーの重イオンを用いたマイクロビーム細胞照射実験系の開発に取り組んでおり、最近、ArイオンやNeイオンによるCHO-K1細胞の核への照射実験を開始した。マイクロビームによる細胞局部照射実験について、過去の数々の試みの歴史を紹介するとともに、特に粒子線マイクロビームを用いた最新の研究状況について述べる。
原田 和樹*; 帯屋 有里乃*; 中野 立央*; 小林 泰彦; 渡辺 宏; 岡市 協生*; 大西 武雄*; 向井 千秋*; 長岡 俊治*
Oncology Reports, 4(4), p.691 - 695, 1997/07
1994年7月にスペースシャトル・コロンビアを用いて実施された第2次国際微小重力実験室(IML-2)において、大腸菌の様々なDNA修復欠損変異株(lexA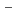 ,recA
,recA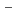 ,urrA
,urrA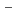 など11種類)の乾燥菌体と、突然変異を検出し易い「ホット・スポット」を有するプラスミドpZ189を、宇宙線飛跡検出器CR-39でサンドイッチした試料を搭載した。飛行後の大腸菌の生存率とプラスミドpZ189上のsupF遺伝子における突然変異誘発頻度を測定し、地上対照実験試料と比較したところ、生存率、突然変異誘発頻度のいずれにおいても、シャトル搭載試料と地上対照実験試料との間で有意の差は見られなかった。すなわち、宇宙で宇宙線による発ガンリスクが高くなることを示唆する結果は得られなかった。
など11種類)の乾燥菌体と、突然変異を検出し易い「ホット・スポット」を有するプラスミドpZ189を、宇宙線飛跡検出器CR-39でサンドイッチした試料を搭載した。飛行後の大腸菌の生存率とプラスミドpZ189上のsupF遺伝子における突然変異誘発頻度を測定し、地上対照実験試料と比較したところ、生存率、突然変異誘発頻度のいずれにおいても、シャトル搭載試料と地上対照実験試料との間で有意の差は見られなかった。すなわち、宇宙で宇宙線による発ガンリスクが高くなることを示唆する結果は得られなかった。
舟山 知夫; 横田 裕一郎; 坂下 哲哉; 鈴木 芳代; 小林 泰彦
no journal, ,
マイクロビーム細胞照射研究グループは、重イオンマイクロビーム生物照射システムの開発と、それを用いた細胞一つ一つに正確に制御したイオンを照射する技術の確立を進めてきた。これまで、サイクロトロンの重イオンビームを四連四重極磁気レンズで集束したビームスポットを顕微鏡下で正確に検出し、スポット位置に細胞を電動ステージで移動することで細胞照準を行ってきたが、この手法を用いる限り、細胞照射のスループットの向上には機械的な限界が伴う。そこで、集束ビームをビームスキャナで高速走査することで、細胞一つ一つに正確かつ高速に重イオンを照射する技術の確立を試みた。CR-39フィルム上に播種したHeLa細胞を生体蛍光染色し、その蛍光画像における位置情報を画像解析で抽出、得られた座標値を元にビームスキャナへの印加電圧を算出し、これを用いて試料への高速走査照射を行った。高速走査照射を行った細胞位置と、CR-39上に可視化したエッチピット位置が合致したこと、および当該細胞への H2AXのフォーカス生成が確認できたことから、照準した細胞への正確な照射を集束ビームの高速走査技術を用いて行うことが可能となったことが確認できた。
H2AXのフォーカス生成が確認できたことから、照準した細胞への正確な照射を集束ビームの高速走査技術を用いて行うことが可能となったことが確認できた。
斎藤 克代*; 舟山 知夫; 小林 泰彦; 村上 孝*
no journal, ,
悪性黒色腫はがんの中でも最も致死性が高い難治性がんの一つであり、化学療法のみならず放射線療法に対しても高い抵抗性を示す。一方で、エピジェネティックな分子標的薬は、遺伝子発現の異常が蓄積しているがん細胞を狙って作用するために、がん選択的な治療効果を高めることができ、高LETの重粒子線は強い抗腫瘍効果が期待できる。そこで本研究では、エピジェネティックな分子標的薬であるヒストン脱アセチル化酵素阻害剤(HDACi)と重粒子線の併用が、悪性黒色腫細胞株に与える影響を、コロニー形成能、細胞増殖能、アポトーシス、細胞周期について検討した。マウス悪性黒色腫細胞株B16F10を複数のHDACiにそれぞれ曝露し、16.5時間後に重粒子線を照射した。コロニーは、照射9( 1)日後にホルマリン固定して染色し、計数した。細胞増殖能, アポトーシス, 細胞周期は、照射36時間後まで経時的に調べた。その結果、HDACiと重粒子線の併用は、悪性黒色腫細胞株B16F10に対して抗腫瘍効果を示した。その効果の程度は投与薬剤によって異なるものの、相乗的な作用が期待できるものが含まれる。
1)日後にホルマリン固定して染色し、計数した。細胞増殖能, アポトーシス, 細胞周期は、照射36時間後まで経時的に調べた。その結果、HDACiと重粒子線の併用は、悪性黒色腫細胞株B16F10に対して抗腫瘍効果を示した。その効果の程度は投与薬剤によって異なるものの、相乗的な作用が期待できるものが含まれる。